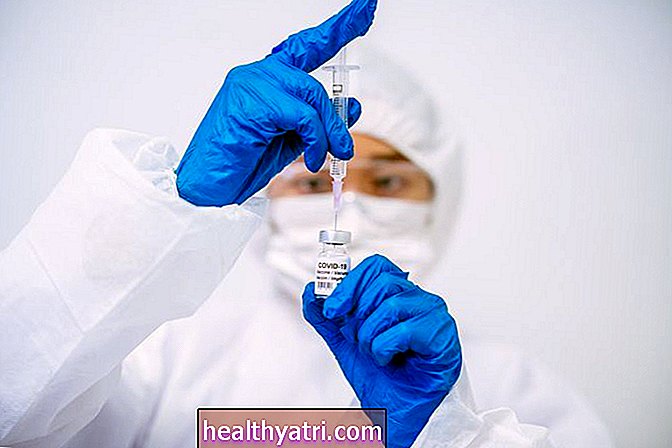
Sasiistock / Getty Images
Ključni zajtrki
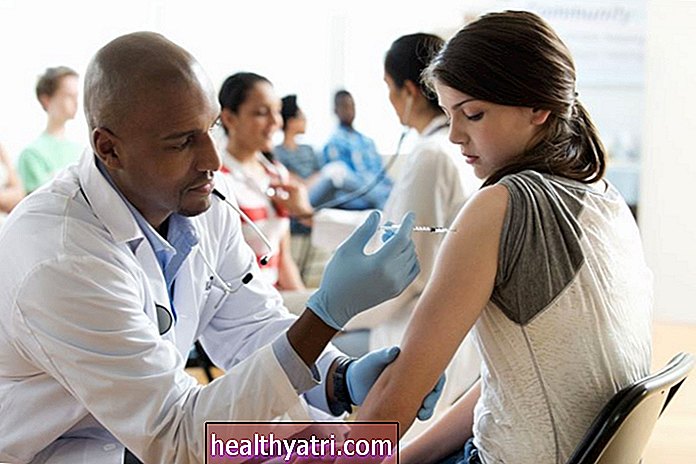
- Pfizer je pridobil odobritev FDA za začetek testiranja cepiva proti koronavirusu pri otrocih, starih 12 let ali več.
- Strokovnjaki pravijo, da je vključevanje otrok v klinična preskušanja ključnega pomena za celoten razvoj cepiva, ki bo tako otroke kot odrasle zaščitilo pred COVID-19.
- Po navedbah na svoji spletni strani je Pfizer v svojo študijo vpisal že več kot 39.000 prostovoljcev. Več kot 34.000 prostovoljcev je že prejelo drugo cepljenje.
Ameriška farmacevtska družba Pfizer je oktobra sporočila, da je od ameriške uprave za hrano in zdravila (FDA) prejela dovoljenje za začetek vključevanja otrok, starih 12 let, v svoja preskušanja cepiva proti koronavirusu.
"S tem bomo lahko bolje razumeli potencialno varnost in učinkovitost cepiva pri posameznikih iz več starosti in okolij," so v posodobljeni izjavi zapisali v podjetju.
To bo prvo preskušanje cepiva COVID-19 v ZDA, ki bo vključevalo otroke. Od oktobra je Pfizer eno od štirih ameriških podjetij, ki imajo cepiva v 3. fazi kliničnih preskušanj.
Pfizer je fazo 3 že razširil na otroke, stare 16 let in več, pa tudi ljudi s kroničnim, stabilnim virusom človeške imunske pomanjkljivosti (HIV), hepatitisom C in hepatitisom B.
Zakaj testirati cepivo COVID-19 pri otrocih?
Preden je Pfizer pridobil odobritev za začetek testiranja pri otrocih, so strokovnjaki v reviji objavili poročiloKlinične nalezljive bolezninavaja pomen takšnega testiranja.
"Neposredni vpliv COVID-19 na otroke je večji kot pri številnih drugih patogenih organizmih, za katere imamo zdaj učinkovita pediatrična cepiva," ugotavlja poročilo. »Poleg tega je bila vloga otrok pri prenosu SARS-CoV-2 očitno podcenjena. S skrbno izvedenimi kliničnimi preskušanji 2. faze se lahko ustrezno rešijo morebitni pomisleki glede varnosti cepiva COVID-19. "
Suzanne Pham, dr.med
Širjenja tega virusa ne moremo premagati, če ne cepimo svojih otrok.
- Suzanne Pham, dr.medSharon Nachman, dr. Med., Vodja oddelka za otroške nalezljive bolezni v Otroški bolnišnici Stony Brook v New Yorku, se strinja s poročilom in je Verywellu povedala, da »pediatri zelo zanimajo podrobnosti študije in kako bo cepivo delovalo pri otrocih. . "
Po Nachmanu ima testiranje cepiva pri otrocih posebne koristi. Raziskovalci bodo lahko ocenili kratkoročni in dolgoročni imunski odziv, kar vključuje tudi ugotovitev, ali je odmerek cepiva, ki se uporablja pri odraslih, potreben za otroke ali pa bi imeli podoben imunski odziv kot nižji odmerek.
Nachman pravi, da je pomembno tudi opozoriti, da bi lahko, preden je koronavirus pri odraslih izpostavljen asimptomatski okužbi pri otrocih, uvedba cepiva za zdravljenje celotne družine "veliko prispevala k zmanjšanju prenosa bolezni doma in v skupnosti."
Suzanne Pham, zdravnica, medicinska sodelavka v bolnišnici Weiss Memorial v Chicagu, za Verywell pove, da prej ko bodo otroci cepljeni, prej se bo stopnja prenosa zmanjšala.
"Z učinkovitim cepljenjem otrok se bo zmanjšalo tveganje, da bodo otroci prenašali virus znotraj skupnosti, zlasti tistim ljudem z visokim tveganjem, ki so bolj dovzetni za hude ali kritične bolezni," pravi Pham za Verywell. »To bo omogočilo, da se šole začnejo znova odpirati in nadzirajo dejavnosti, ki so ključne za razvoj naših otrok. Širjenja tega virusa ne moremo premagati, če ne cepimo svojih otrok. V družbi moramo imeti dovolj čredne imunosti, da lahko preprečimo širjenje. "
Cepiva COVID-19: Bodite na tekočem, katera cepiva so na voljo, kdo jih lahko dobi in kako varna so.
Kako se začnejo preskusi s cepivi?
Pham pojasnjuje, da mora podjetje za testiranje cepiva - na odraslih ali otrocih - FDA najprej vložiti vlogo za raziskovalno novo zdravilo (IND).
Vloga bo opisala cepivo, način njegove izdelave in preskuse kakovosti. Vloga vključuje tudi podatke iz preskusov na živalih, ki dokazujejo, da je cepivo varno za začetno testiranje na ljudeh.
Kot pojasnjuje FDA, ima postopek prijave več korakov:
Med zgodnjim predkliničnim razvojem novega zdravila je glavni cilj sponzorja ugotoviti, ali je izdelek primerno varen za začetno uporabo pri ljudeh in ali ima spojina farmakološko aktivnost, ki upravičuje komercialni razvoj.
Ko je izdelek opredeljen kot izvedljiv kandidat za nadaljnji razvoj, se sponzor nato osredotoči na zbiranje podatkov in informacij, potrebnih za ugotovitev, da izdelek pri omejenih kliničnih študijah v zgodnji fazi ne bo izpostavljal ljudi nerazumnim tveganjem.
Nato bodo cepivo opravili preskuse faze 1, za katere Pham pojasnjuje, da so "študije varnosti in imunogenosti, opravljene pri majhnem številu ljudi, ki jih pozorno spremljajo."
"Faza 2 je sestavljena iz študij glede odmerjanja in je razširjena na večje število (na stotine) ljudi," pravi Pham. "Nato skušajo poskusi 3. faze vključiti na tisoče ljudi, da dokumentirajo učinkovitost in še naprej preučujejo varnostne podatke."
Po navedbah na svoji spletni strani je Pfizer v svojo študijo vključil več kot 39.000 prostovoljcev. Več kot 34.000 jih je prejelo drugi odmerek cepiva.
Kaj to pomeni za vas
Klinično preskušanje 3. faze, ki vključuje testiranje cepiva COVID-19 pri otrocih, je znak napredka. Vendar s cepivom ni mogoče hiteti. Za dokončno oblikovanje rezultatov je potreben čas za zaščito varnosti udeležencev preskušanja ter odraslih in otrok, ki bodo sčasoma prejeli končno različico cepiva.






.jpg)
.jpg)









.jpg)