VioletaStoimenova / Getty Images
Ključni zajtrki
- FDA tesno sodeluje s proizvajalci pri podatkih o varnosti in učinkovitosti, ki jih pričakuje, da bi razmislila o odobritvi cepiva COVID-19.
- FDA načrtuje sklic zunanjega svetovalnega odbora za pregled podatkov o vsakem cepivu COVID-19, ki je vloženo v dovoljenje.
- Podjetja, ki dobijo dovoljenje za uporabo cepiva COVID-19 v sili, morajo nadaljevati s kliničnimi preskušanji, da bodo lahko dolgoročno zagotavljala informacije o varnosti in učinkovitosti.
- FDA pričakuje, da bodo podjetja, ki jim je bilo izdano dovoljenje za uporabo v sili, vložila tudi standardno odobritev, ki ni nujna.
Danes je uprava za hrano in zdravila (FDA) drugič v enem tednu sklicala Svetovalni odbor za cepiva in sorodne biološke izdelke, da priporoči „dovoljenje za nujno uporabo“ (EUA) za novo cepivo COVID-19, ki ga je izdelala Moderna.
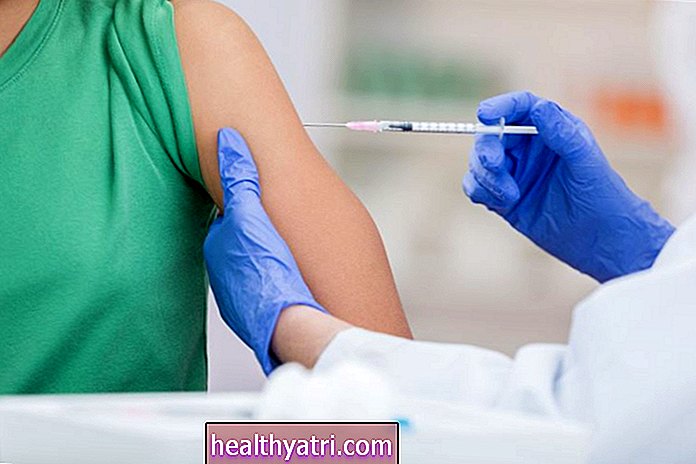
Prvo cepivo proti COVID-19, ki ga je izdelala družba Pfizer-BioNTech, je FDA odobrila prejšnji teden, prejšnji ponedeljek pa so se v ZDA začela cepljenja nekaterih zdravstvenih delavcev - prvih ljudi, imenovanih za cepivo.
Kaj pa je pravzaprav EUA?
Program EUA je bil ustanovljen leta 2004, po terorističnem napadu v ZDA 11. septembra 2001, da bi dovolil uporabo neodobrenega medicinskega izdelka ali neodobrene uporabe odobrenega medicinskega izdelka med razglašenim izrednim dogodkom na področju javnega zdravja. COVID-19 je 31. januarja 2020 kot izredni dogodek na področju javnega zdravja v ZDA vzpostavil minister za zdravje in socialne zadeve Alex Azar.
Cepiva COVID-19: Bodite na tekočem, katera cepiva so na voljo, kdo jih lahko dobi in kako varna so.
"Ko je razglašena nujna situacija, lahko FDA presodi, da je vredno dati nekaj v uporabo, tudi brez vseh dokazov, ki bi v celoti ugotovili njeno učinkovitost in varnost," je za Verywell povedal Joshua Sharfstein, nekdanji glavni namestnik komisarja FDA. . Sharfstein je zdaj prodekan za prakso javnega zdravja in sodelovanje na šoli za javno zdravje Johns Hopkins Bloomberg v Baltimoru v zvezni državi Maryland.
EUA so bili prej izdani za zdravila ali cepiva za zdravljenje ali preprečevanje antraksa, ebole in bližnjevzhodnega respiratornega sindroma (MERS), pravi Sharfstein.
Zahteve za prijavo EUA
Proizvajalec se lahko prijavi za EUA - v nasprotju s formalnejšo odobritvijo vloge za dovoljenje za biološka zdravila (BLA) - če ni na voljo drugega cepiva, ki bi preprečilo stanje. Poleg tega se mora FDA odločiti, da znane in potencialne koristi cepiva odtehtajo tveganje njegovega prejema.
"[Za EUA] je na splošno manj podatkov, kot bi bili na voljo za [a BLA]," pravi LJ Tan, glavni strateški direktor koalicije za imunizacijsko akcijo, zagovorniške skupine, ki si prizadeva za povečanje stopnje imunizacije v ZDA, . "To pa ne pomeni, da so klinična preskušanja pri načrtovanju ogrožena. Samo EUA je izdan prej kot dovoljenje, zato za preskušanje še ne bomo nabrali toliko podatkov."
Po navedbah FDA morajo biti izdelki, predloženi za EUA, še vedno strogo testirani. Oktobra je FDA delila industrijske smernice glede tega, kaj bi iskali glede podatkov o varnosti in učinkovitosti cepiv COVID-19, vključno s podatki iz študij o varnosti cepiva, ter vsaj dva meseca spremljanja po kliničnem preskušanju. dokončanja.
V skladu s smernicami lahko FDA odobri EUA za cepivo, če:
- Izdelek lahko razumno prepreči, diagnosticira ali zdravi tako resne ali življenjsko nevarne bolezni ali stanja, ki jih lahko povzroči SARS-CoV-2.
- Znane in potencialne koristi odtehtajo znana in potencialna tveganja.
- Za diagnosticiranje, preprečevanje ali zdravljenje bolezni ali stanja izdelka ni ustrezne, odobrene in razpoložljive alternative.
FDA pričakuje, da bodo proizvajalci cepiv vključili načrt za spremljanje varnosti cepiva - ki vključuje preiskovanje vseh poročil o smrtnih primerih, hospitalizacijah in drugih resnih ali klinično pomembnih neželenih dogodkih - med posamezniki, ki prejmejo cepivo pod EUA.
"Biti odprt in jasen glede okoliščin, v katerih bi bilo izdajanje dovoljenja za uporabo v sili za cepivo COVID-19 ključnega pomena za krepitev zaupanja javnosti in zagotovitev uporabe cepiv COVID-19, ko bodo na voljo," Peter Marks, dr. Doktor znanosti, direktor Centra za vrednotenje in raziskave bioloških zdravil FDA, je dejal v izjavi. "Poleg tega, da opišemo naša pričakovanja do sponzorjev cepiv, upamo tudi, da smernice agencije o cepivih COVID-19 javnosti pomagajo razumeti naš znanstveno utemeljen postopek odločanja, ki zagotavlja kakovost, varnost in učinkovitost cepiv za katero koli cepivo, ki je odobreno ali odobreno . "
FDA tudi pričakuje, da bodo proizvajalci, ki prejmejo EUA, nadaljevali s kliničnimi preskušanji in na koncu vložili zahtevek za BLA. EUA ne velja več, ko razglasitev izrednih razmer na področju javnega zdravja ne bo več veljala, kar pomeni, da bo za nadaljnjo uporabo cepiva potrebna popolna odobritev.
Kaj to pomeni za vas
Uprava za prehrano in zdravila dovoljuje podjetjem, da zaprosijo za dovoljenje za zdravilo COVID-19 po postopku, imenovanem dovoljenje za nujno uporabo, ki lahko pospeši čas, potreben za odobritev cepiva.